口罩出口资质与申报条件详解
伴随着全球对防疫用品需求的持续上升,口罩已成为重要的出口商品。对于有意向出口口罩的企业,了解并满足相关的资质与申报条件是顺利开展国际贸易的关键。本文将针对一次性口罩的出口,详细梳理所需的资质与申报流程。
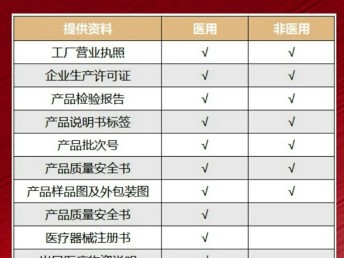
一、 出口前必须取得的国内资质
- 营业执照:企业经营范围需包含相关医疗器械或劳保用品的生产与销售。
- 医疗器械产品注册证与生产许可证:若出口的是一次性医用口罩,生产企业必须向国家药品监督管理局申请并获得《医疗器械产品注册证》和《医疗器械生产许可证》。这是证明产品安全有效、符合中国质量标准的法定文件。
- 检测报告:口罩需通过具备资质的检测机构检验,并获得合格的检测报告,证明其符合中国国家标准(如GB 19083-2010医用防护口罩、YY 0469-2011医用外科口罩、GB/T 32610-2016日常防护型口罩)或相应的国际/目的国标准。
- 非医用口罩声明:若出口的是一次性非医用防护口罩(如日常防护口罩),企业需进行自我声明,承诺产品符合中国质量标准或合同约定的标准,并准备相应的质量检测报告以备查验。
二、 出口申报通关的核心条件
- 对外贸易经营者备案:企业需在所在地商务主管部门完成备案,取得进出口经营权。
- 海关报关单位注册登记:向海关申请办理注册登记,获取报关资格。
- 商品检验:口罩属于法定检验商品,出口前需向海关申报实施商品检验。企业需提交合同、发票、装箱单、检测报告、医疗器械注册证(如适用)等单证。海关将审核单证并对货物进行查验,确保产品符合质量安全要求。自2021年6月起,对部分医疗物资(包括医用口罩)实行出口商品检验。
- 报关单证准备:齐全、准确的报关单证是顺利通关的基础,主要包括:合同、发票、装箱单、报关单、代理报关委托书(如委托报关)、上述提及的各类资质证书与检测报告等。
- 目的国准入要求:这是至关重要的环节。出口企业必须提前了解并满足目的国家或地区的市场准入条件,这可能包括:
- 当地认证:如美国的FDA认证(医用口罩需510(k)或EUA授权)、欧盟的CE认证(需符合相关指令和协调标准,并由公告机构发证或进行符合性自我声明)、日本的PMDA认证等。
- 进口商资质:目的国进口商可能需要具备特定的药品或医疗器械经营许可。
- 标签与说明书:产品包装、标签和说明书需符合目的国的语言、内容及格式要求。
三、 一次性口罩出口特别注意事项
- 准确归类:在报关时,必须根据口罩的材质、用途(医用或非医用)准确归类海关商品编码(HS Code),这直接关系到监管条件、税率和所需提交的单证。例如,医用口罩通常归入品目6307,而非医用口罩可能归入品目6307或3926等。
- 质量是生命线:全球市场监管日趋严格,劣质口罩不仅面临退货、销毁、罚款风险,更会损害“中国制造”声誉。确保从原材料到成品的全过程质量控制至关重要。
- 关注动态政策:国内外针对防疫物资的贸易政策可能动态调整,企业应密切关注中国海关总署、商务部、国家药监局以及目的国监管机构发布的最新通告和指南。
一次性口罩的出口是一项涉及生产质量、国内法规和国际贸易规则的系统性工作。企业需夯实产品质量基础,取得完备的国内资质,并深入研究目标市场法规,准备好全套合规文件,才能确保口罩顺利出口,在国际市场上行稳致远。
如若转载,请注明出处:http://www.kangchugs.com/product/87.html
更新时间:2026-05-20 22:30:59